ポイント
- 舌がんの免疫プロファイルを詳細に解析し、がん微小環境の特徴を明らかに
- 舌がんの免疫特性に基づき、患者ごとに五つの免疫サブタイプに分類
- 免疫サブタイプごとに適した治療法を検討することで、個別化医療の実現に貢献
概要
東京科学大学(Science Tokyo)※大学院医歯学総合研究科 顎口腔腫瘍外科学分野および口腔科学センターの蘇郁雅大学院生(博士後期課程)、原田浩之教授、東みゆき名誉教授、臨床腫瘍学分野の加納嘉人講師、頭頸部外科学分野の朝蔭孝宏教授らの研究グループは、富山大学 医学薬学教育部 生命・臨床医学専攻の大内崚大学院生(博士課程)、野口誠名誉教授の研究グループと共同で、舌扁平上皮がん[用語1]のがん微小環境がん微小環境[用語2]における包括的免疫プロファイル解析を行い、免疫サブタイプをIからVの五つに分類しました。
がん微小環境における免疫細胞の集積やその多様性は、がん治療、特に免疫チェックポイント阻害薬[用語3]による免疫療法の効果に大きく影響します。現在、再発・転移頭頸部がんに対しては、抗 PD-1[用語4]抗体であるニボルマブやペムブロリズマブの使用が承認されています。しかし、その効果は悪性黒色腫(メラノーマ)や非小細胞性肺がんと比べると十分とは言えません。特に、舌は動く器官であり、日々の生活の中で外界からの刺激を受けやすいため、免疫抑制作用が働きやすいという特性があります。
本研究では、87例の未治療手術検体を用い、58項目にわたる包括的免疫プロファイル解析を実施しました。さらに、細胞傷害性T細胞(CTL)[用語5]とがん細胞の空間的解析を行い、免疫サブタイプを五つに分類しました。その結果、免疫プロファイルはTNM分類[用語6]からは推測できず、患者ごとに異なることが明らかになりました。また、 免疫チェックポイント阻害薬の効果が期待できる免疫賦活型の割合は 16.1% にとどまり、残りのサブタイプでは何らかの免疫抑制が起こっていることが分かりました。この免疫サブタイプ分類は、免疫チェックポイント療法の適応可否を判断する上で有用であり、さらに他の免疫療法や化学療法との併用戦略を検討する際にも役立つと考えられます。
本研究の成果は、舌がんにおける個別化医療を促進し、より多くの患者に対して最適な治療法の選択を可能にすることで、治療成績の向上に貢献すると期待されます。
本成果は3月1日付で、国際的ながん免疫療法学会の複合機関誌「Cancer Immunology, Immunotherapy」に掲載されました。
- 2024年10月1日に東京医科歯科大学と東京工業大学が統合し、東京科学大学(Science Tokyo)となりました。
背景
頭頸部がんは、鼻腔、口腔、咽頭、喉頭(のど)などにできるがんです。なかでも、口腔がんの頻度は高く、口腔がんの中では舌がんが最も多く見られます。舌がんの治療は、TNM分類およびその総合的評価(Stage)、さらに病理組織の結果に基づき、治療法の選択や予後の予測が行われています。
近年、免疫抑制状態を解除することを目的とした免疫チェックポイント阻害薬による免疫療法が、頭頸部がんを含むさまざまな再発・転移がんに対して利用されるようになりました。しかし、免疫チェックポイント阻害薬の効果は全てのがん患者に認められるわけではなく、単剤投与ではなく他の治療法との併用が必要になるケースも多くあります。
免疫チェックポイント阻害薬の効果に最も大きく影響する要因は、がん微小環境における免疫プロファイル、すなわち、がん細胞の周囲にどのような種類の免疫細胞が、どの程度の密度で、どのような空間配置で存在しているかです。この免疫プロファイルは、がんの種類によって異なるだけでなく、同じがん種であっても個人によって大きく異なります。
現在、PD-1免疫チェックポイント阻害薬の効果予測には、PD-1と結合する相手分子であるPD-L1の発現スコア(TPS, CPS)が一般的に用いられていますが、これだけでは十分に信頼できる指標とは言えません。また、舌は動いている器官であり、日常的に外界からの刺激を受けるため、免疫抑制の作用が強く働きやすい特性を持っています。
そこで本研究では、舌がんの大半を占める舌扁平上皮がんを対象に、がん微小環境の免疫プロファイルを解析し、治療法の選択や予後予測に活用できる免疫サブタイプ分類の確立を試みました。
研究成果
舌扁平上皮がんと診断され、化学療法や放射線療法などの前治療を受けずに舌切除手術を受けた87例の患者を対象に、マルチプレックス免疫蛍光染色[用語7]と定量組織イメージ解析システムを用いて免疫プロファイル解析を実施しました。この手法では、わずか2枚の組織切片を用いることで、7つの異なる免疫細胞サブセットの分布(密度と比率)を特定すると同時に、PD-1およびPD-L1の発現比率を解析することができます。
本研究では、58項目にわたる免疫パラメーターを評価し、免疫パラメーターの相関関係に基づいて階層分類を行いました。その結果、全ての免疫細胞に発現するCD45陽性免疫細胞密度(Leukocyte-density, Leu-D)、細胞傷害性T細胞(CTL)と制御性 T細胞(Treg)を除いたヘルパーT細胞(conventional helper T, Tcon)の比率 (C/Tcon%)、およびCTL%を指標に、まず以下の三つのタイプに分類しました(図1)。
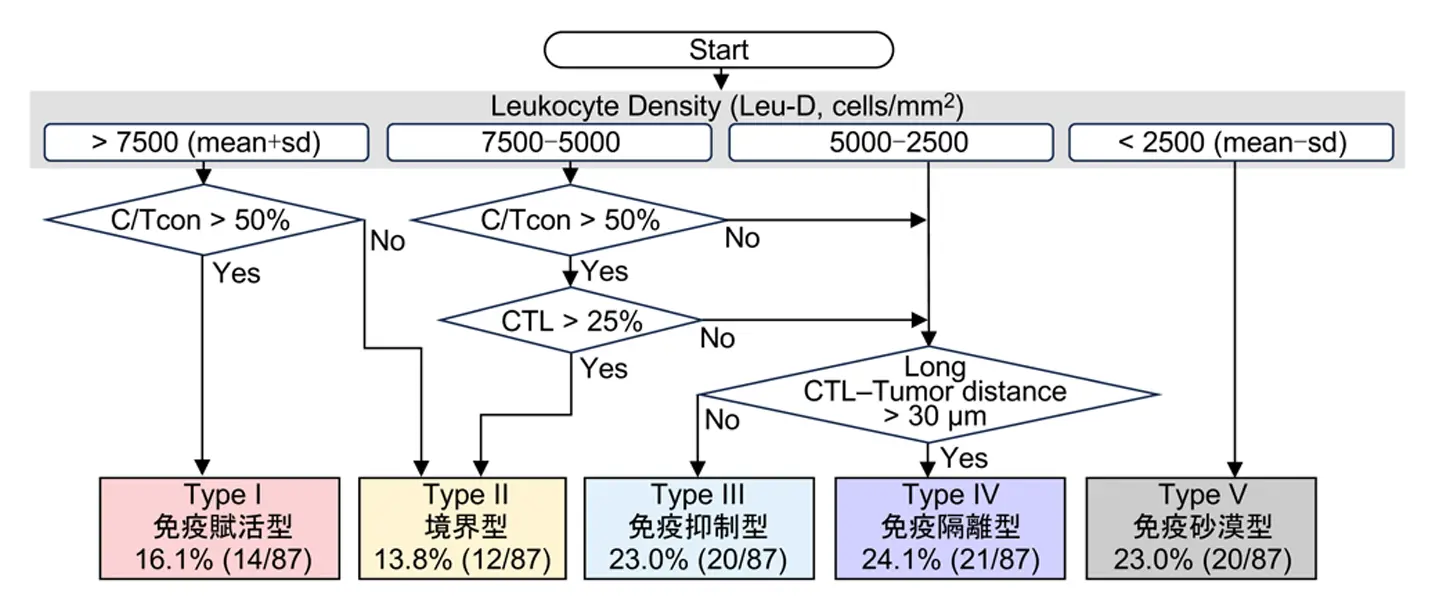
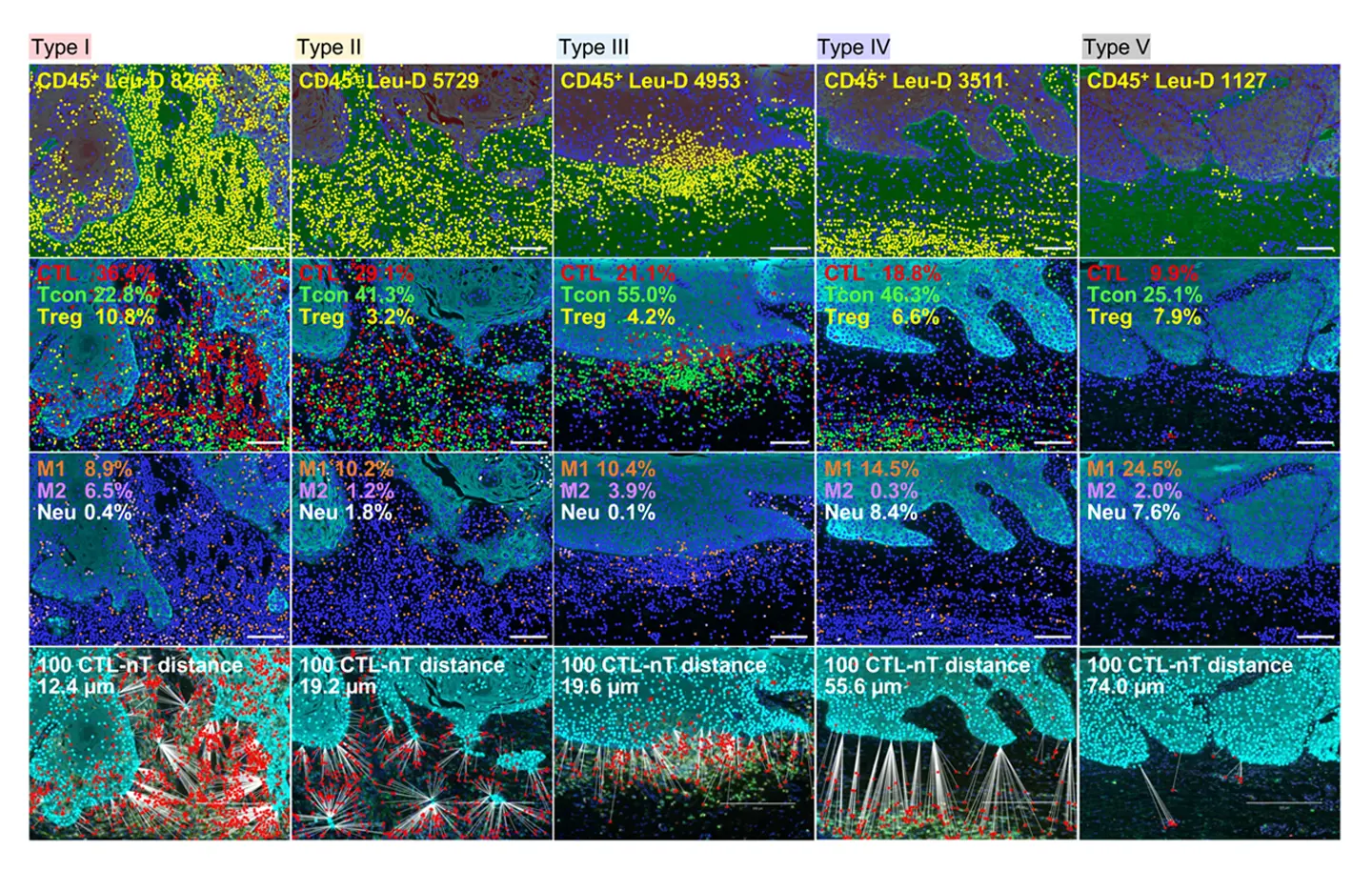
- 免疫賦活型(Type I):免疫細胞密度および C/Tcon 比率が高いタイプ
- 境界型(Type II):免疫細胞密度はType I ほどではないものの、C/Tcon 比率 およびCTL比率が高いタイプ
- 免疫砂漠型(Type V):免疫細胞浸潤が極端に少ないタイプ
次に、これらに分類されなかった症例について、CTL とがん細胞の距離をイメージ解析し、以下の 二つのタイプに分類しました。
- 免疫抑制型(Type III):CTL 密度は高いが、免疫抑制細胞である制御性 T 細胞やマクロファージの密度が高いタイプ
- 免疫隔離型(Type IV):CTL ががん細胞に近づけない環境にあるタイプ。がん関連線維芽細胞(CAF)やがん細胞が産生する免疫抑制因子の影響が考えられる
87症例の解析の結果、免疫賦活型(Type I)は 16.1%にとどまり、免疫抑制型(Type III)が23.0%、免疫隔離型(Type IV)が24.1%、免疫砂漠型(Type V)が23.0%を占め、 70%以上が積極的な免疫応答が見られない、つまり免疫応答が制御されているタイプであることが分かりました。
免疫サブタイプ間の比較では、Leu-D(免疫細胞密度)および CTL-D(CTL 密度)は、免疫タイプが進むにつれて減少していました(図2)。なお、本研究の免疫サブタイプ分類にはPD-1やPD-L1の発現は使用していませんが、PD-1およびPD-L1の発現解析の結果、以下の関係が明らかになりました。
- PD-1 発現 CTL 密度はマクロファージ密度と相関
- PD-L1 発現マクロファージ密度は CTL 密度と相関
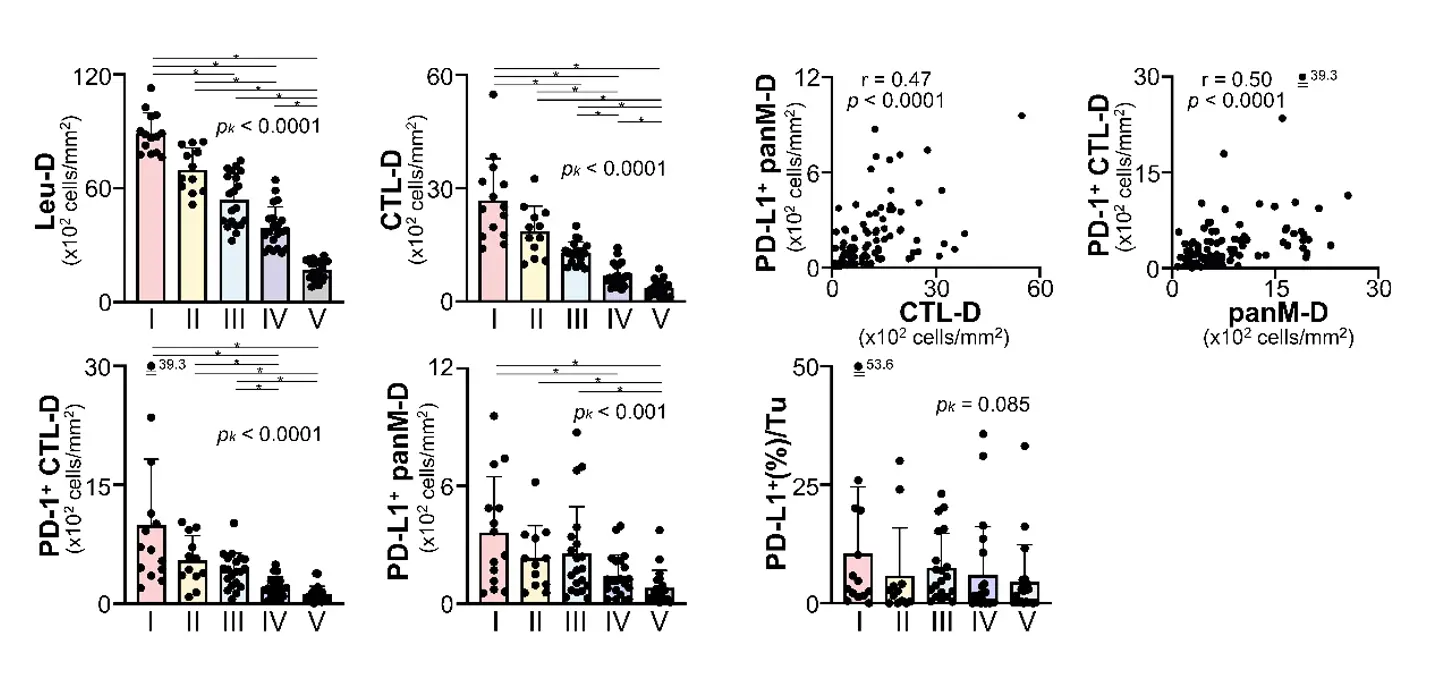
また、PD-1発現CTL密度およびPD-L1発現マクロファージ密度は、タイプが進むにつれて低下していました。一方、PD-L1発現がん細胞の比率については、タイプ間で大きな変化は見られませんでした。これらの結果から、PD-1発現 T細胞はマクロファージ浸潤と関連し、がん浸潤マクロファージのPD-L1発現はCTL浸潤と関連していることが示されました。さらに、免疫賦活型(Type I)は免疫チェックポイント療法の感受性が高いことが推察されました。
免疫賦活型では、5年予後において再発・転移が発生していませんでした。また、免疫チェックポイント療法を受けた再発・転移17例の免疫プロファイル解析では、免疫賦活型(Type I)は存在せず、約半数が免疫砂漠型(Type V)に分類されました。Type IIIからType Vでは、それぞれ特有の免疫制御が起こっていることが示唆されており、タイプごとに適した免疫併用療法の選択が必要であると考えられました。
社会的インパクト
現在、頭頸部がんにおける免疫チェックポイント阻害薬の適用は、再発・転移症例に限られています。しかし、術前補助療法や術後補助療法としての臨床試験も進められています。本研究で確立した舌がんの免疫サブタイプ分類は、免疫チェックポイント阻害薬の使用にとどまらず、一次治療の治療法選択にも有用であると考えられます。
さらに、再発・転移症例においては、免疫チェックポイント阻害薬を単独で使用するべきか、また併用が必要な場合はどの薬剤を選択すべきかを判断する指標としても活用できる可能性があります。本研究の成果は、舌がんの個別化医療の発展に貢献し、より適切な治療戦略の確立につながると期待されます。
今後の展開
本研究では、包括的な免疫プロファイル解析を実施しましたが、最終的に免疫サブタイプ分類に使用したのは、がん増殖最先端におけるCD45およびCD8陽性細胞の分布でした。CD45およびCD8の免疫染色に加え、通常の診断でルーチンに実施されているH&E染色があれば、病理医が五つの免疫サブタイプに分類することが可能です。
今後、この舌がんの免疫サブタイプ分類が多施設で標準的に実施され、舌がん治療のガイドラインに取り入れられることが期待されます。本研究の成果は、舌がんの個別化医療を推進し、より多くの患者の治療成績向上に貢献すると考えられます。
付記
本研究は、文部科学省科学研究費助成事業(18H04066、21H03138)の支援を受けて実施されました。
用語説明
- [用語1]
- 舌扁平上皮がん:口腔がんに含まれ、舌粘膜表面の扁平上皮から発生する癌で舌癌のほとんどを占める。
- [用語2]
- がん微小環境:正常とは異なる癌周囲特有の局所環境。
- [用語3]
- 免疫チェックポイント阻害薬:TLA-4, PD-1あるいは PD-L1などのT細胞免疫抑制性分子に対するヒト化抗体で、がん免疫治療薬として利用されている。
- [用語4]
- PD-1:T細胞上に発現し、そのリガンド PD-L1結合によりT細胞抗原受容体からのシグナルを抑制することができる細胞表面タンパク受容体分子である。リガンドPD-L1は、癌細胞やマクロファージに発現誘導される。
- [用語5]
- 細胞傷害性T細胞(CTL):CD8陽性のT細胞で、癌細胞を直接傷害することのできるキラーT細胞。
- [用語6]
- TNM分類:癌の大きさ(T)、リンパ節転移の程度(N)、遠隔転移(M)からなるがんの進行度を評価する国際的分類で、治療方針を決定する際の基準として使用される。
- [用語7]
- マルチプレックス免疫蛍光染色:多重免疫蛍光染色の手法であるが、組織に結合した抗体を取り除き、蛍光色素のみを残していくことで、何種類もの分子を同一切片で同定することができる。
論文情報
- 掲載誌:
- Cancer Immunology, Immunotherapy
- タイトル:
- Stratification of the immunotypes of tongue squamous cell carcinoma to improve prognosis and the response to immune checkpoint inhibitors
- 著者:
- Yuya Su, Ryo Ouchi, Pissacha Daroonpan, Miwako Hamagaki, Tohru Ikeda, Noji Rika, Naoto Nishii, Fumihiko Tsushima, Yoshihito Kano, Takahiro Asakage, Makoto Noguchi, Hiroyuki Harada, Miyuki Azuma
研究者プロフィール
蘇 郁雅 Yuya SU
東京科学大学 大学院医歯学総合研究科 顎口腔腫瘍外科学分野 大学院生
研究分野:口腔外科学

大内 崚 Ryo OUCHI
富山大学 医学薬学教育部 生命・臨床医学専攻 大学院生
研究分野:口腔外科学

原田 浩之 Hiroyuki HARADA
東京科学大学 大学院医歯学総合研究科 顎口腔腫瘍外科学分野 教授
研究分野:口腔外科学

東 みゆき Miyuki AZUMA
東京科学大学 大学院医歯学総合研究科 顎口腔腫瘍外科学分野 非常勤講師
口腔科学センター 顧問
東京医科歯科大学 名誉教授
研究分野:免疫学、口腔外科学

関連リンク
お問い合わせ
東京科学大学 口腔科学センター 顎口腔腫瘍外科学分野
東 みゆき
- miyuki.mim@tmd.ac.jp
富山大学 医学薬学教育部 生命・臨床医学専攻
大内 崚
- Tel
- 076-434-7383
- Fax
- 076-434-5041
取材申し込み
富山大学 総務部 総務課 広報・基金室
- kouhou@u-toyama.ac.jp
- Tel
- 076-445-6028
- Fax
- 076-445-6063
東京科学大学 総務企画部 広報課
- media@adm.isct.ac.jp
- Tel
- 03-5734-2975
- FAX
- 03-5734-3661