ポイント
- 遺伝性パーキンソン病の原因遺伝子がコードするDJ-1タンパク質が、有害な細胞内代謝物cPGAの分解酵素として働く仕組みを世界で初めて解明
- 構造モデリングや生化学的解析により、cPGA分解反応に必要なDJ-1のアミノ酸残基を特定し、分解メカニズムを分子レベルで解明
- パーキンソン病患者に見られるDJ-1の疾患関連変異が、cPGA分解機能を完全に喪失させることを実証
- DJ-1によるcPGA分解の生理的意義を細胞レベルで検証し、DJ-1の機能破綻がパーキンソン病発症に関与する新たな分子病態メカニズムを提唱
概要
東京科学大学(Science Tokyo) 総合研究院 難治疾患研究所 機能分子病態学分野の松田憲之教授と、同研究所 計算創薬科学分野の森脇由隆准教授らの研究チームは、遺伝性パーキンソン病の原因遺伝子DJ-1(PARK7)[用語1]がコードするDJ-1タンパク質が、糖の代謝過程で生じる有害な副生成物 cPGA (cyclic 3-phosphoglyceric anhydride)[用語2]を分解する酵素として働く仕組みを、初めて明らかにしました。さらに、遺伝性パーキンソン病患者が持つ変異によって、このDJ-1の酵素機能が損なわれることも明らかにしました。
本研究は、DJ-1のcPGA分解酵素としての機能が破綻することが、パーキンソン病の発症につながる可能性を示唆しています。これは、パーキンソン病発症の新たな病態メカニズムを提唱するものであり、今後の創薬ターゲットの同定に貢献することが期待されます。
本研究は、東京科学大学の渡辺藍子プロジェクト研究員、荻原禅大学院生、齋藤未怜大学院生、山科雅裕助教、小谷野史香講師、山野晃史准教授、石谷隆一郎教授、東京薬科大学の三島正規教授、東京都立大学の伊藤隆教授、東京都医学総合研究所の田中啓二理事長、徳島大学の小迫英尊教授との共同研究であり、研究成果は2025年6月4日付(現地時間)に、米国の科学雑誌「Journal of Cell Biology」に掲載されました。
背景
パーキンソン病は進行性の神経変性疾患であり、運動機能に障害を引き起こします。その多くは孤発性に発症しますが、遺伝性のパーキンソン病も存在します。DJ-1は遺伝性パーキンソン病の原因遺伝子であり、その機能が失われると病気が発症することから、通常はパーキンソン病の発症を抑えている「パーキンソン病の抑制遺伝子」とされています。DJ-1タンパク質の細胞内での機能については、これまでさまざまな役割が提唱されてきましたが、「生理的に本当に重要な機能」は長年不明のままでした。今回、松田憲之教授らは、DJ-1タンパク質が有害な細胞内代謝物であるcPGAを分解する酵素であることを証明し、さらにその反応機構を分子レベルで解明しました。
研究成果
-
DJ-1はcPGAを加水分解する酵素活性を持つ
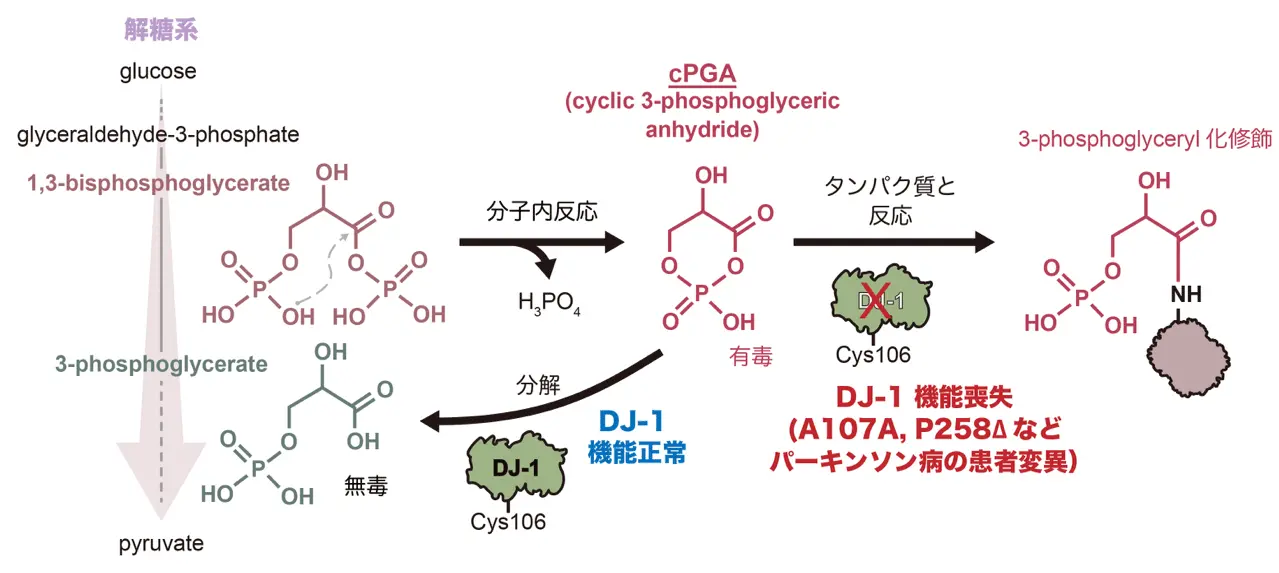
DJ-1が、反応性代謝物であるcPGAを分解し、無害な物質である3-ホスホグリセリン酸を生成する反応の詳細を、構造モデリングと生化学的解析により明らかにしました。具体的には、DJ-1の求核性システインC106[用語3]、オキシアニオンホールG74/G75[用語4]、A107、P158、E18(cPGAとの相互作用部位)などの残基が、cPGAの分解反応を触媒する過程でどのように働くかを示しました。さらに、パーキンソン病患者にみられる変異であるA107PおよびP158Δ[用語5]が、DJ-1のcPGA分解酵素活性を完全に喪失させることを明らかにしました。 -
細胞内での生理的意義の検証
Phos-tagゲル[用語6]を用いた独自の検出法や質量分析による解析から、DJ-1が欠損した細胞では、cPGA由来の修飾が異常に蓄積することが示されました。この結果により、細胞内におけるcPGAの解毒にはDJ-1が不可欠であることが実証されました。 -
グリオキサラーゼ活性との比較
従来、DJ-1はメチルグリオキサールを解毒するグリオキサラーゼ活性を持つことが代表的な分子機能と考えられてきました。DJ-1は試験管内ではこの反応を触媒しますが、細胞内ではDJ-1が欠損してもメチルグリオキサールは蓄積せず、代わりにcPGAが蓄積することが示されました。この結果により、細胞内におけるcPGAの解毒にはDJ-1が不可欠であることが実証されました。
社会的インパクト
本研究では、DJ-1がcPGA分解酵素であり、DJ-1の失活が強い毒性を持つ代謝物cPGAの蓄積を引き起こすことを、分子レベルで解明しました。これにより、若年性パーキンソン病の発症メカニズムの理解が一歩進展しました。将来的には、cPGAを測定することでパーキンソン病の発症リスクを評価できる可能性や、DJ-1の酵素活性を補完する創薬戦略の確立につながる可能性が期待されます。
また、本研究で確立された「DJ-1とcPGAの相互作用モデル」や「Phos-tagゲルを用いたcPGA修飾の可視化技術」は、他の反応性代謝物の研究や、神経変性疾患における代謝ストレスの理解にも応用可能です。
今後の展開
- DJ-1の酵素機能を活性化する低分子化合物の探索
- cPGAの蓄積によって引き起こされる神経障害機構のさらなる解明
- 本研究で確立した「反応性代謝副産物を検出する技術」の、他の代謝ストレスに起因する疾患への応用と展開
付記
本研究は、日本学術振興会科学研究費助成事業、日本医療研究開発機構 AMED-CREST「翻訳後修飾によるオルガネラ・ホメオスタシスの分子機構と生理作用の解明」、武田科学振興財団、日本医療研究開発機構(AMED) 生命科学・創薬研究支援基盤事業BINDS(課題番号 JP24ama121012、JP24ama121027)、東京科学大学難治疾患共同研究拠点経費、高深度オミクス医学研究拠点整備事業、学際領域展開ハブ形成プログラムの助成を受けて実施されました。
用語説明
- [用語1]
- DJ-1(PARK7):遺伝性潜性パーキンソン病の原因遺伝子の一つ。これまで、抗酸化酵素や解毒酵素としての機能が注目されてきた。
- [用語2]
- cPGA(cyclic 3-phosphoglyceric anhydride):糖の代謝過程で生じる高反応性の中間代謝物。タンパク質や他の代謝物に非特異的な修飾を加えることで、細胞障害を引き起こす。
- [用語3]
- 求核性システインC106:電子を供与する性質を持つシステイン。加水分解酵素の反応中心として機能する。
- [用語4]
- オキシアニオンホールG74/G75:加水分解酵素の触媒部位に存在し、反応中間体を安定化させるうえで重要な構造要素。
- [用語5]
- A107PおよびP158Δ変異:DJ-1に生じるパーキンソン病の原因変異。本研究により、いずれの変異も酵素活性の喪失を引き起こすことが初めて示された。
- [用語6]
- Phos-tagゲル:リン酸化修飾を受けたタンパク質を、移動度の違いによって可視化できるゲル電気泳動技術。本研究では、cPGA修飾の検出に初めて応用された。
論文情報
- 掲載誌:
- Journal of Cell Biology
- タイトル:
- The reaction mechanism for glycolysis side product degradation by Parkinson's disease-linked DJ-1
- 著者:
- Aiko Watanabe, Shizuka Ogiwara, Mirei Saito, Masaki Mishima, Masahiro Yamashina, Ryuichiro Ishitani, Yutaka Ito, Keiji Tanaka, Fumika Koyano, Koji Yamano, Hidetaka Kosako, Yoshitaka Moriwaki, and Noriyuki Matsuda
研究者プロフィール
松田 憲之 Noriyuki MATSUDA
東京科学大学 総合研究院 難治疾患研究所 機能分子病態学分野 教授
研究分野:遺伝性パーキンソン病の発症機構の解明