ポイント
- 半世紀近くにわたり実現していなかったナフトサイクリノン類の化学合成法を開発。
- 独自に開発した合成法を特徴的な橋架け構造の構築に活用。
- 異なる構造を持つ誘導体の合成にも展開可能な合成経路を開発。
概要
東京科学大学(Science Tokyo)※理学院 化学系の安藤吉勇准教授、星野大樹大学院生(研究当時)、大森建教授、鈴木啓介栄誉教授(同 総合研究院 基礎研究機構 特命教授)らの研究チームは、天然由来の有機化合物ナフトサイクリノン類の世界初の全合成[用語1]に成功しました。
ナフトサイクリノン類は、1974年にドイツの研究者A. Zeeckらによって放線菌から単離された天然物[用語2]で、ピラノナフトキノンが2つの化学結合を介して二量化した特徴的な橋架け構造[用語3]を有しています。しかし、構造決定から半世紀近くが経っても、その構造の複雑さから化学合成は未到のままでした。
本研究では、合成化学的な難問である、不斉炭素[用語4]を含む橋架け構造の立体選択的[用語5]な構築法を独自に開発することによって、β-ナフトサイクリノンとγ-ナフトサイクリノンという2種類のナフトサイクリノン類の全合成を達成しました。本成果は、他のナフトサイクリノン類の合成に応用できるだけでなく、今後、異なる様式の橋架け構造を持つ天然物の合成への展開も期待できます。
本成果は、11月12日付(現地時間)の「Angewandte Chemie International Edition」誌に掲載されました。
- 2024年10月1日に東京医科歯科大学と東京工業大学が統合し、東京科学大学(Science Tokyo)となりました。
背景
天然物の全合成研究は、植物や細菌などが産生する有機化合物(天然物)を入手容易な原料から人工的に化学合成する、「ものづくり」の研究分野です。自然界にある天然物の化学構造には、単純なものから複雑なものまで多種多様なものがあります。化学者は、あるときは純粋な好奇心から、またあるときは社会的要請から天然物を合成してきました。天然物の提示する分子構造の合成化学的課題を解決することは、有機化学分野の発展につながります。その中で開発された分子構築法や不斉合成法は、薬や機能性材料の創出を通して人類に恩恵をもたらしてきました。一方で、人間が合成できる分子構造は現代においても限られており、複雑精緻な化学構造を持つ天然物を人工的に合成することは簡単ではありません。そのため、天然物合成を通した合成化学的問題の解決と、それに伴う新しい合成手法の開発は常に求められています。
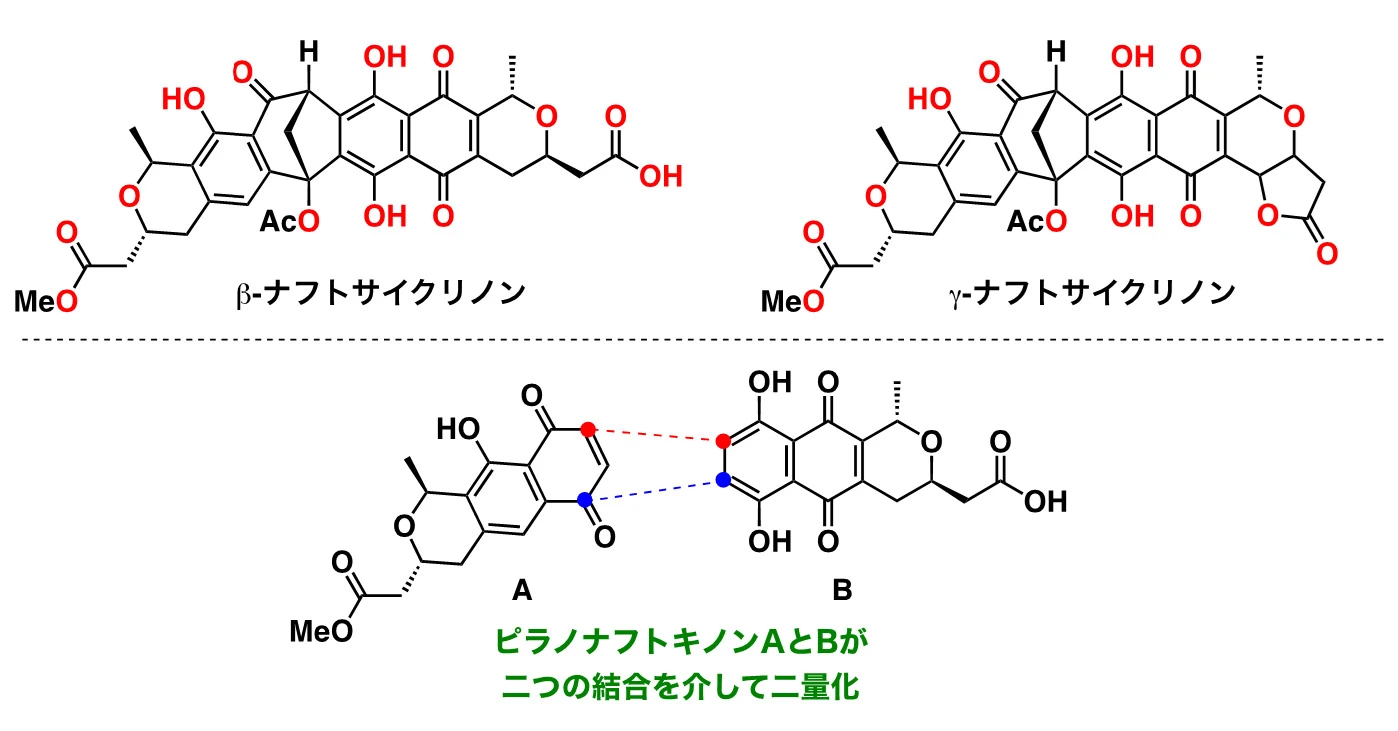
ナフトサイクリノン類は、1974年にドイツの研究者A. Zeeckらによって、カメルーンの火山火口付近の土壌に生息する放線菌から単離された天然物で、β-ナフトサイクリノンやγ-ナフトサイクリノンなど、8種が知られています(図1)。多環性の骨格が多くの酸素原子(赤で表示)で修飾された構造に加えて、ピラノナフトキノンAおよびBが2つの化学結合を介して二量化した特徴的な橋架け構造を有しており、合成化学者の注目を集めていました。しかし、構造決定の報告から半世紀近くが経つにも関わらず、その構造の複雑さから化学合成は未到のままでした。
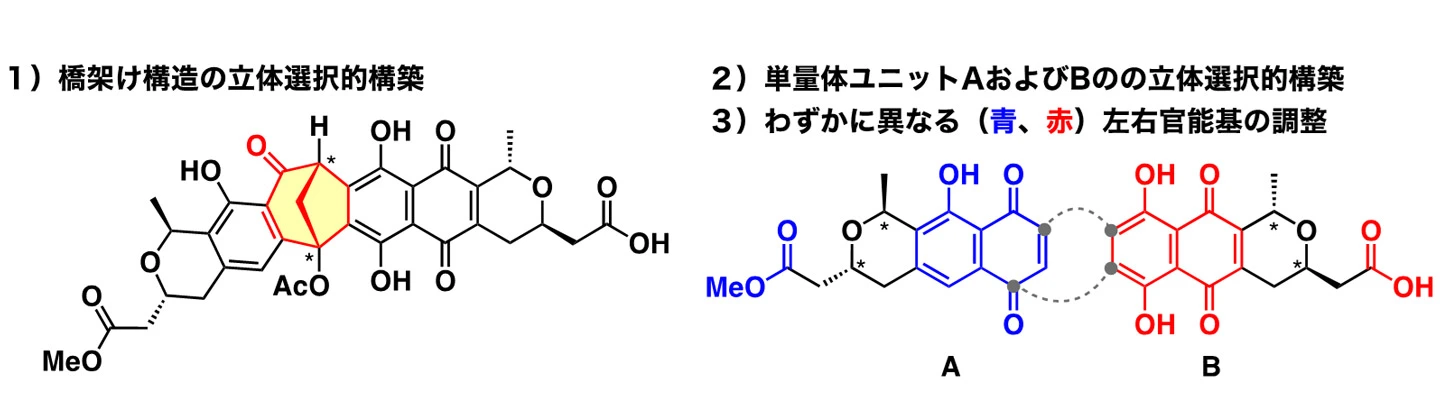
その合成には次のような合成化学的課題があります(図2)。
-
橋架け構造の立体選択的構築
ナフトサイクリノン類に特徴的な橋架け構造(黄色部分)は、構築自体が難しいですが、その不斉炭素を立体選択的に合成することはいっそう困難です。 -
単量体構造の立体選択的構築
二量体構造の構成要素である単量体のピラノナフトキノンAおよびBも不斉炭素を有しています。この不斉炭素も立体選択的に合成することが求められます。 -
非対称な二量体構造に由来する官能基の調節
左右の単量体構造(ピラノナフトキノン)AおよびBの持つ官能基はわずかに異なっています(青と赤で対比)。これらの違いを化学反応により選択的に整えていくことは簡単ではありません。
全合成を実現するには、こうした個々の課題を解決しつつ、それらの整合性をとることが求められます。
研究成果
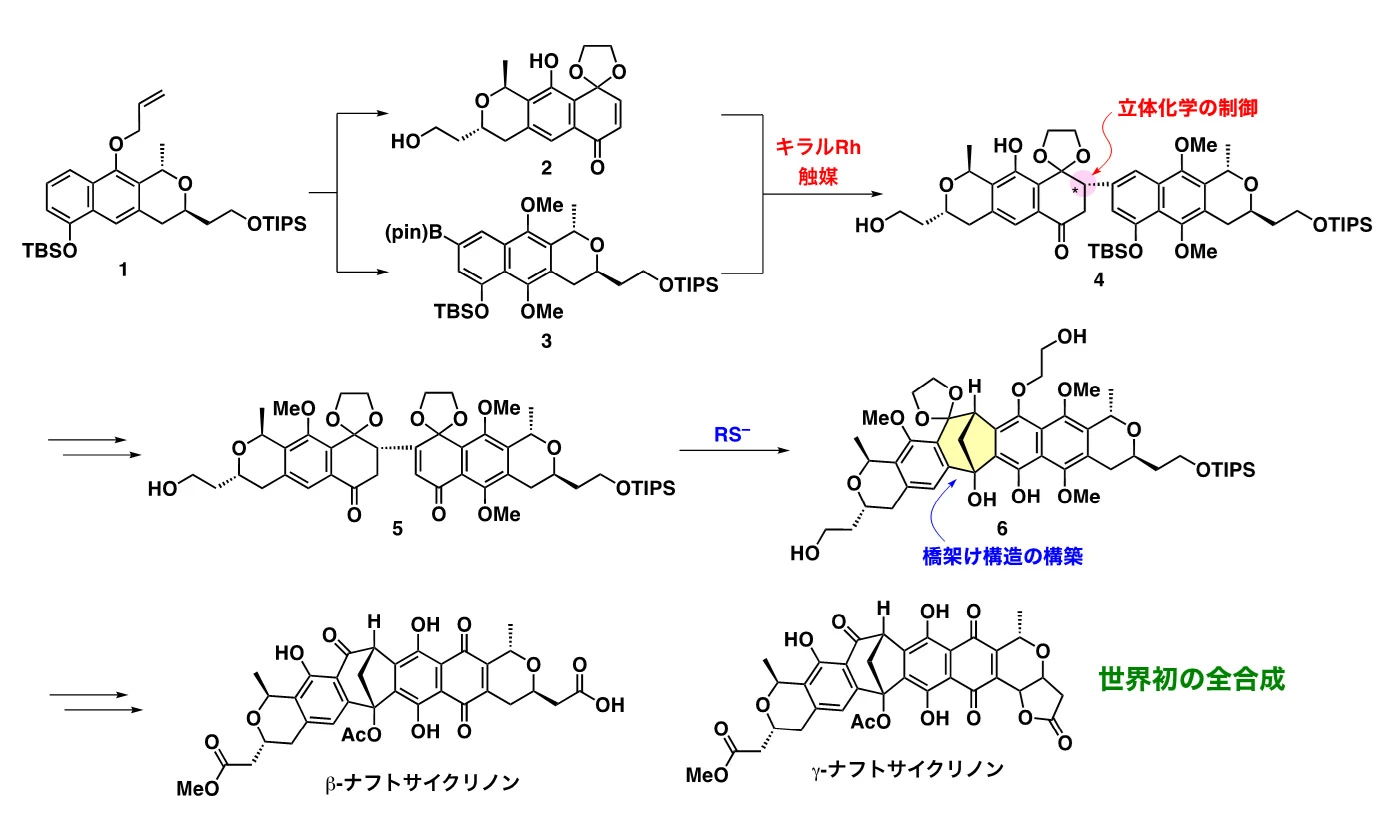
本研究では、ナフトサイクリノン類が提示する合成化学的課題を解決するために、独自の合成戦術と戦略を開発し、それらを駆使して、β-ナフトサイクリノンとγ-ナフトサイクリノンの全合成を達成しました(図3)。
この全合成の過程においてはまず、ピラノナフタレン1を設計し、独自に開発した立体選択的な合成法により調製しました[参考文献1]。次に、これを共通の中間体として、単量体ユニット2と3をそれぞれ合成しました。これらを、キラルロジウム触媒を用いた不斉1,4-付加反応により連結することで、付加体4を立体選択的に合成することができました[参考文献2]。
この付加体4の官能基を変換することにより、環化前駆体5へと導きました。この5に対して、硫黄原子の反応性を活用した環化反応を行うことで、橋架け構造を構築することに成功し、ビシクロ化合物6を合成できました。この変換反応は、ナフトサイクリノン合成のために我々が独自に開発したものです[参考文献3]。その特徴は、硫黄原子が求核剤[用語6]と還元剤[用語7]の2つの役割を担うことにあります。これまで、同様の橋架け構造を持つ、天然物の合成に本手法が適用できることは分かっていました[参考文献2]。今回、より複雑な骨格にも利用できたことで、汎用性の高い変換法であることが分かりました。
最後に、このビシクロ化合物6の左右の官能基を選択的に変換することで、β-ナフトサイクリノンとγ-ナフトサイクリノンへ導くことができました。これにより、約半世紀前に単離・構造決定された歴史的な天然物の全合成に世界で初めて成功したことになります。
社会的インパクトと今後の展開
本成果によって、ナフトサイクリノン類の合成法が開拓されたことで、他の類縁体合成も可能になると期待できます。また、今回開発した新たな合成手法は、他の橋架け構造を持つ天然物の合成にも展開できます。
今回の研究成果は、人類が合成可能な化学構造の選択肢を広げることにつながり、医薬品開発や材料化学研究に必要な物質の供給のための基盤になると期待されます。今後の研究でも引き続き、天然物合成における合成化学的な問題を解決し、有機合成化学の発展に貢献していきます。
付記
本研究は、科学研究費助成事業(課題番号:23000006, JP16H06351, JP19K05452, JP21H04703, JP23H04888)、東京工業大学・研究の種発掘支援、武田科学振興財団ライフサイエンス研究助成、戸部眞紀財団研究助成の支援を受けて行われました。
用語説明
- [用語1]
- 全合成:入手容易な化学物質(バイオマスや化石資源由来)から化学反応を駆使して、天然物を化学合成すること。
- [用語2]
- 天然物:主に生物が産生する有機化合物の総称。身近な例では、アミノ酸やグルコース、ビタミンCなども天然物である。
- [用語3]
- 橋架け構造:有機化合物を構成する原子(主に炭素)の骨格様式のひとつ。ビシクロ構造とも呼ぶ。2つの環状構造が2つ以上の原子を共有している骨格様式のことである。単純な環状構造に比べて合成が難しい。
- [用語4]
- 不斉炭素:炭素原子は4つの化学結合を持つことができる。この4つの結合につながる置換基の種類が全て異なる場合、その炭素原子は「不斉炭素」と呼ばれ、不斉炭素を持つ有機化合物には鏡像異性体(エナンチオマー)が存在する。多くの有機化合物にはこの不斉炭素が存在する。
- [用語5]
- 立体選択的:分子構造に不斉炭素が複数存在すると、その組み合わせの数に応じた立体異性体が想定されうる。例えば、不斉炭素が3つあると2×2×2=8種類の立体異性体が存在する。立体選択的合成とは、複数考えられる立体異性体の中から1つだけを優先して得られるようにする化学合成のことである。
- [用語6]
- 求核剤:一般的な有機反応は、正(プラス)電荷を持つものと負(マイナス)電荷を持つものが静電引力により新しい結合を生成する。このとき、正電荷を持つものを求電子剤、反対に負電荷を持つものを求核剤と呼ぶ。
- [用語7]
- 還元剤:「還元」とは物質が電子を獲得する反応のことである。電子を供給することができる反応剤を還元剤と呼ぶ。
参考文献
- [1]
- Y. Ando, M. M. Maturi, T. Hoshino, N. Tanaka, T. Sakai, K. Ohmori, K. Suzuki, Synlett 2023, 34, 2011.
- [2]
- T. Fukazawa, Y. Ando, K. Ohmori, T. Hayashi, K. Suzuki, Org. Lett. 2017, 19, 1470.
- [3]
- Y. Ando, S. Hori, T. Fukazawa, K. Ohmori, K. Suzuki, Angew. Chem. Int. Ed. 2015, 54, 9650.
論文情報
- 掲載誌:
- Angewandte Chemie International Edition
- 論文タイトル:
- Total Synteses of β- and γ-Naphthocyclinones
- 著者:
- Yoshio Ando*, Taiju Hoshino, Nozomi Tanaka, Mark M. Maturi, Yusuke Nakazawa, Takumi Fukazawa, Ken Ohmori*, Keisuke Suzuki
研究者プロフィール
安藤吉勇 Yoshio ANDO
東京科学大学 理学院 化学系 准教授
研究分野:有機合成化学、天然物合成、反応開発
大森建 Ken OHMORI
東京科学大学 理学院 化学系 教授
研究分野:有機合成化学、天然物合成
鈴木啓介 Keisuke SUZUKI
東京科学大学 栄誉教授/同 総合研究院 基礎研究機構
研究分野:有機合成化学、天然物合成、反応開発